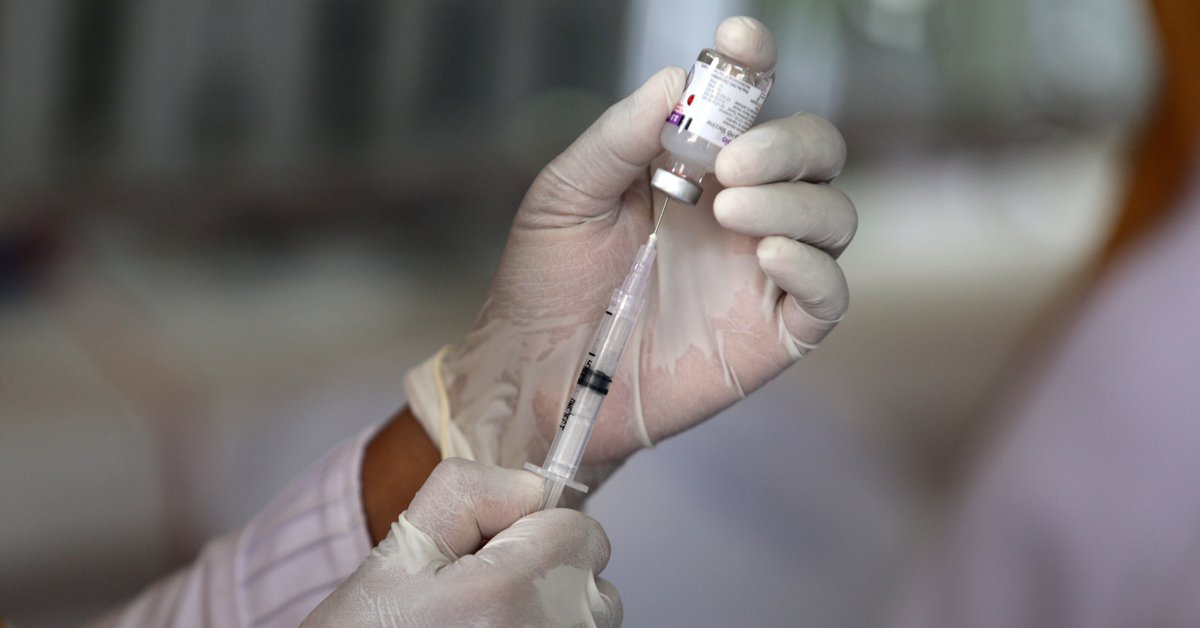
El gigante farmacéutico Pfizer continúa avanzando en las pruebas de su vacuna COVID-19 y Para fines de noviembre, espera solicitar la autorización de emergencia para la distribución del medicamento a la Administración de Drogas y Alimentos de los Estados Unidos (FDA). Según lo declarado por el director general de la empresa, Albert Burla.
«Permítanme ser claro, si los datos son positivos, Pfizer solicitará autorización de emergencia en los EE. UU., Poco después de que finalice la fase de seguridad, en la tercera semana de noviembre».Informar al gerente en una carta abierta.
La farmacéutica estadounidense es una de las tres empresas con las que México firmó acuerdos de compra el 13 de octubre. Según el secretario de Hacienda, el convenio contempla la compra de entre 15,5 y 34,4 millones de vacunas contra el SARS-CoV-2 a Pfizer, cuyos medicamentos requieren dos aplicaciones, y llegarán al país en diciembre. Sin embargo, antes de que esto suceda, la multinacional debe demostrar que su tratamiento cumple con las tres condiciones exigidas por la Administración de Alimentos y Medicamentos.
Hay tres áreas principales en las que, como con todas las vacunas, debemos demostrar el éxito para obtener la aprobación para uso general. primero, La vacuna debe demostrar su eficaciaEs decir, puede ayudar a prevenir el COVID-19 en la mayoría de los pacientes que han sido vacunados durante al menos un segundo y, lo que es más importante, Debe probarse que es seguro, Con datos de seguridad sólidos generados a partir de miles de pacientes. Finalmente, debemos demostrar que “Se puede producir de manera constante con los más altos estándares de calidad”, dijo el CEO.

Desde la empresa esperan verificar la efectividad de la vacuna a fines de octubre, Por lo que habrían completado la primera condición. Un equipo de científicos independientes se encargará de analizar los resultados y determinar la efectividad del fármaco, que Pfizer ha desarrollado con la empresa alemana BioNTech.
Podemos saber si nuestra vacuna es efectiva o no a fines de octubre. Para hacer esto, debemos agrupar una cierta cantidad de casos de COVID-19 en nuestro experimento, para comparar la efectividad de la vacuna en individuos vacunados con aquellos que recibieron un placebo. «Dado que tenemos que esperar a que ocurra una cierta cantidad de casos, estos datos pueden llegar tarde o temprano», dijo Burla en el comunicado.
“Dado que Pfizer no sabe quién recibió la vacuna y quién recibió el placebo, un panel de científicos independientes revisará los datos completos y nos informará si es eficaz o no.«, agregó.
Probar la eficacia de la vacuna es solo el primer requisito. Entonces tendrán que demostrar que también es seguro. Para hacer esto, la Administración de Alimentos y Medicamentos Se necesitan dos meses desde que se inyectó la segunda y última dosis a los participantes del ensayo clínico, con el fin de monitorear los posibles efectos adversos durante ese tiempo. Según los datos que maneja Pfizer, completarán este plazo en la tercera semana de noviembre, y solo entonces podrán solicitar el permiso de emergencia.
Nuestros estándares internos con respecto a la seguridad de las vacunas y requeridos por los reguladores son altos. En el caso de que se obtenga autorización de emergencia en Estados Unidos para una posible vacuna contra COVID-19, La Administración de Alimentos y Medicamentos requiere que las empresas proporcionen datos de seguridad durante dos meses para la mitad de los participantes del ensayo, después de proporcionar la dosis final de la vacuna. Basándonos en nuestro índice actual de pruebas y dosis, estimamos que alcanzaremos este hito en la tercera semana de noviembre ”, reveló el CEO.
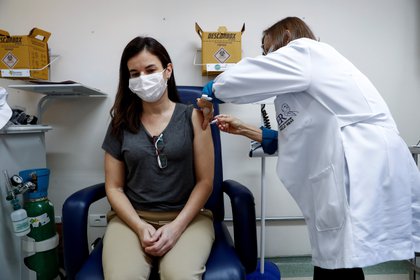
Finalmente, deberán demostrar su capacidad para producir la vacuna a gran escala. Según Burla, podrán facilitar estos datos antes de que finalice la fase de seguridad, es decir, antes de la tercera semana de noviembre.
El requisito final será proporcionar datos de fabricación que demuestren la calidad y consistencia de la vacuna. Pfizer ha estado invirtiendo en riesgo desde que la pandemia comenzó a mejorar nuestros procesos de fabricación, La capacidad aumenta rápidamente. Esperamos que nuestros datos de fabricación estén listos para su envío antes de llegar a la etapa de seguridad «.
Con eso, a fines de noviembre, Estados Unidos podría tener dos vacunas listas para su distribución, ya que Moderna planea lanzarlas también en esa fecha.
Acuerdos de compra en México

Esta semana, el gobierno mexicano anunció la firma de acuerdos de compra con tres empresas farmacéuticas que trabajan en una vacuna contra COVID-19: La empresa estadounidense Pfizer, la empresa británica AstraZeneca y la china CanSinoBio. Estos contratos, valorados en $ 1.659 millones, con la plataforma Kovacs de la OMS, protegerán a 116 millones de mexicanos.
«Pagaremos la entrega (…) Durante diciembre, se pueden vacunar hasta 2,6 millones de personas; Luego, 3,5 millones de personas adicionales entre enero y febrero; Y 11 millones de personas en marzo.El ministro de Hacienda del país, Arturo Herrera, quien también informó que el primer lote llegará en diciembre, será provisto por empresas estadounidenses y asiáticas.
En total, se acordó la compra de 77,4 millones de dosis de AstraZeneca; Entre 15,5 y 34,4 millones para Pfizer y 35 millones para CanSinoBio. Según el ministro de Salud, Jorge Alcoser, la aplicación dará prioridad al personal médico que lucha contra enfermedades y grupos vulnerables.
Más sobre este tema:
Vacuna COVID-19 en México: ¿Quién será el primero en recibirla en el primer trimestre de 2021?
Coronavirus en México: confíe en AMLO para iniciar la vacunación en diciembre
¿Cómo pagará México la vacuna COVID-19?

«Experta en zombis. Entusiasta del tocino. Practicante de Twitter. Evangelista de televisión. Ninja de Internet. Gurú del café incondicional».




More Stories
Juez rechaza intento de bloquear la administración de Biden Prohibición de acuerdos de no competencia
A medida que más escombros de turbinas llegan a Nantucket, la ciudad está considerando presentar una demanda
Cómo la ‘regla de las dos pizzas’ de Jeff Bezos puede ayudarle a alcanzar el éxito financiero